Ajatus siitä, että kaikki maailman aineet koostuvat atomista, syntyi 5. vuosisadalla eKr., Kun antiikin Kreikan ajattelija Democritus ehdotti, että kaikki olemassa oleva koostuu pienimmistä liikkuvista hiukkasista. Voitaisiin vain olettaa, että todennäköisimmin sillä ei ole merkitystä. Monien vuosisatojen ajan demokratian jälkeen atomit muistutettiin ajoittain, mutta tämä hypoteesi ei ollut suosittu noina aikoina. 1800-luvulla atomihypoteesi esiintyi tieteellisellä horisontilla.
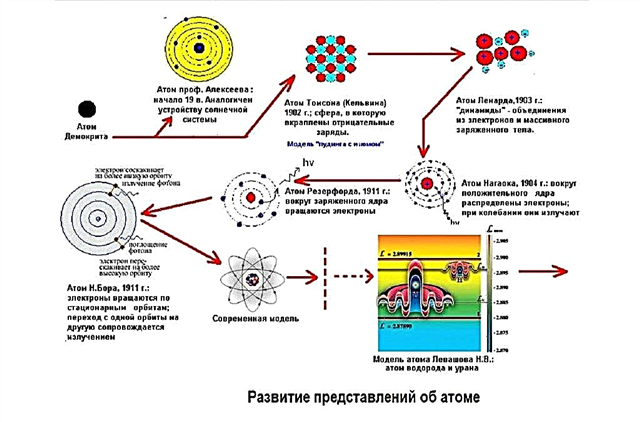
Atomien rakennemallit

Tutkijat etsivät mallia, joka pystyisi kuvaamaan tyydyttävästi kuvan todellisesta maailmasta. Atomi osoittautui erittäin sopivaksi malliksi. Vaikka atomeja ei voida nähdä, mutta antamalla niiden olemassaolon, tutkijat pystyivät selittämään, mitä he havaitsivat kokeissaan ja luonteeltaan.
Tutkijat olivat vakuuttuneita atomien olemassaolosta kauan ennen kuin he pystyivät todistamaan sen. Malli toimi, vaikka kukaan ei pystynyt todistamaan sen totuutta. Esimerkiksi 1800-luvun alkupuolella englantilainen tiedemies John Dalton, tutkiessaan kemiallisten reaktioiden lakeja, havaitsi, että kaksi ainetta reagoi aina kemiallisesti samalla vakioosuudella. Esimerkiksi yhden osan happea ja kahden osan vetyä yhdistelmä antaa vettä.
Tämä viittasi siihen, että yhden aineen atomit, joiden massa on yhtä suuri kuin toiset, liittyivät toisen aineen (ts. Eri massan atomien) atomiin. Veden muodostumisen tapauksessa yksi happiatomi yhdistyy kahdella vetyatomilla.Atomimalli auttoi ymmärtämään, mitä Dalton tarkalleen havaitsi kokeissaan. Atomien olemassaolosta on myös yksinkertaista näyttöä.
Jos katsot mikroskooppia siitepölyhiukkasista, jotka ovat suspendoituneet veteen, voit nähdä, että ne tekevät kaoottisia liikkeitä. Miksi? Tutkijat ovat väittäneet, että tämä voi johtua siitä, että siitepölyhiukkaset törmäävät lukuisiin atomiin tai atomiryhmiin, joita tutkijat ovat kutsuneet molekyyleiksi (esimerkiksi vedessä olevat hiukkaset törmäävät vesimolekyyleihin).
Mistä atom koostuu?
Atomiteorian kanssa yhtä mieltä olleet tutkijat uskoivat, että atomi koostuu pienistä sähköisesti varautuneista hiukkasista - positiivisista ja negatiivisista, jotka yhdistettynä atomiin, kuten pallo, neutraloivat toisiaan ja tekevät atomista kokonaan sähköisesti neutraalin. Mutta vuonna 1907 englantilainen fyysikko Ernest Rutherford osoitti kokeiluillaan, että tämä ei ole täysin totta.
Rutherford-kokemus
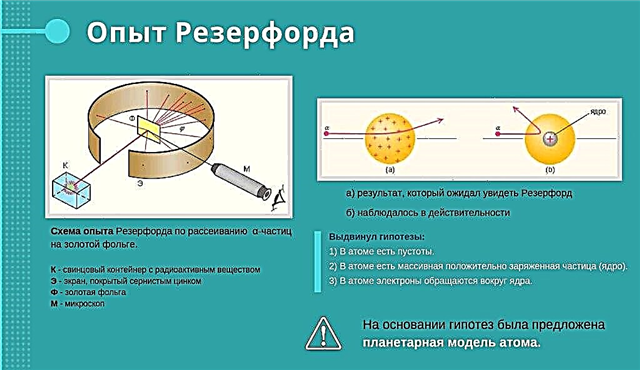
Rutherford pommitti kultafolioa positiivisen varauksen omaavien hiukkasten nopean säteen kanssa. Hän uskoi hiukkasten kulkevan folion läpi. Jotkut positiivisesti varautuneet hiukkaset lentävät folion läpi. Ja jotkut eivät voineet tehdä tätä. Lisäksi he rikoksiittivat kokeilijaan, kuin jos folioon piilotettu voima työntäisi heidät pois. Rutherford oli yllättynyt. Hän sanoi, että se oli samaa kuin alkaa polttaa ruukku kuitupaperille ja yhtäkkiä nähdä, kuinka ruukku lentää potterin otsasta.
Planetaarinen atomimalli - atomin ydin
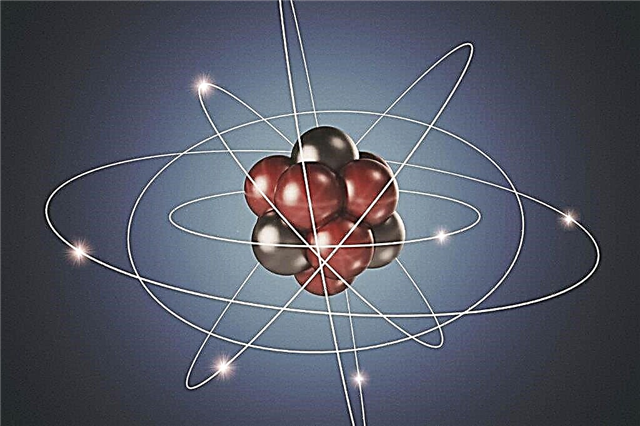
Rutherfordin kokeilut auttoivat vahvistamaan atomihypoteesin ja ymmärtämään atomin toimintaa. Kävi selväksi, että positiiviset ja negatiiviset hiukkaset eivät ole jakautuneet tasaisesti atomissa. Jos näin olisi, niin positiivisesti varautuneita hiukkasia Rutherford-kokeessa ei hylätään sellaisella voimalla. Siksi atomin ydin ei ole neutraali. Atomin keskellä on tiheä hiukkasten pallo, ts. Keskellä, jota kutsutaan atomin ytimeksi, ovat positiivisesti varautuneita protoneja ja neutraaleja neutroneja.
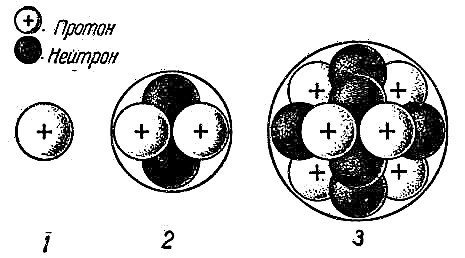
Huomattavan etäisyyden päässä ytimestä, negatiivisesti varautuneet hiukkaset - elektronit - pyörivät sen kiertoratojen ympärillä. Koska positiivinen varaus on yhtä suuri kuin negatiivinen varaus, atomi on kokonaisuutena sähköisesti neutraali. Se ei sisällä mitään maksuja.
Mutta ydin itsessään on positiivisen varauksen keskittyminen. Monet Rutherfordin kokeilun positiivisista hiukkasista lensivat liian lähelle kultaatoman positiivisesti varautuneita ytimiä. Koska positiiviset varaukset hylkivät toisiaan, nämä hiukkaset lentävät takaisin kohti kokeilijaa. Tämä sai hänet ajatukseen siitä, kuinka atomit tosiasiallisesti järjestetään.
Kvarkkien
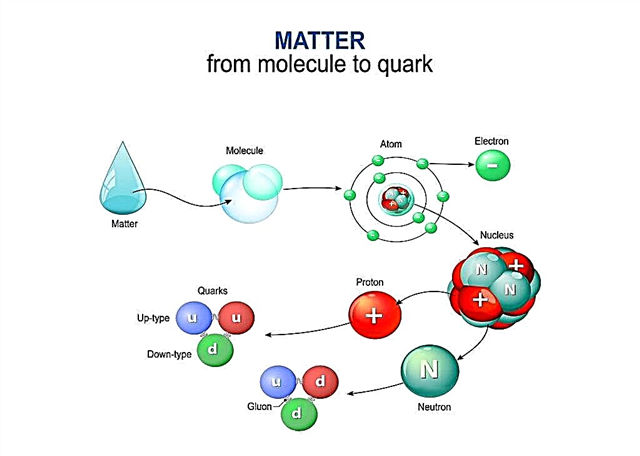
Protonit ja neutronit ovat hiukkasia, jotka, vaikka ovatkin pieniä, koostuvat vielä pienemmistä partikkeleista, joita kutsutaan kvarkeiksi. Nykyään tutkijat uskovat, että protonit ja neutronit koostuvat vielä pienemmistä hiukkasista, joita kutsutaan kvarkeiksi.
Kvarkit ovat uusi malli, joka selittää paremmin atomien käyttäytymistä todellisessa maailmassa. Ja aivan kuten tutkijat olivat aiemmin etsineet kokeellista näyttöä atomien olemassaolosta, nyt he etsivät todellista vahvistusta kvarkkien olemassaololle.












